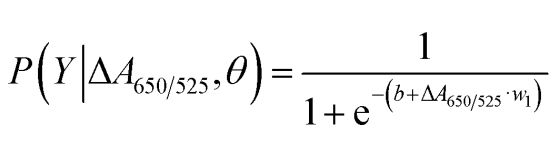თხევადი ბიოფსიის საფუძველზე კიბოს ადრეული გამოვლენა კიბოს გამოვლენისა და დიაგნოსტიკის ახალი მიმართულებაა, რომელიც ბოლო წლებში აშშ-ის ეროვნული კიბოს ინსტიტუტმა შემოგვთავაზა, კიბოს ადრეული ან თუნდაც კიბოსწინარე დაზიანებების აღმოჩენის მიზნით. ის ფართოდ გამოიყენება, როგორც ახალი ბიომარკერი სხვადასხვა ავთვისებიანი სიმსივნეების, მათ შორის ფილტვის კიბოს, კუჭ-ნაწლავის სიმსივნეების, გლიომებისა და გინეკოლოგიური სიმსივნეების ადრეული დიაგნოსტიკისთვის.
მეთილაციის ლანდშაფტის (Methylscape) ბიომარკერების იდენტიფიცირების პლატფორმების გაჩენას აქვს პოტენციალი, მნიშვნელოვნად გააუმჯობესოს კიბოს ადრეული სკრინინგის არსებული მეთოდები, რაც პაციენტებს მკურნალობას ადრეულ ეტაპზე გადაიყვანს.
ცოტა ხნის წინ, მკვლევარებმა შეიმუშავეს მეთილირების ლანდშაფტის აღმოჩენის მარტივი და პირდაპირი სენსორული პლატფორმა, რომელიც დაფუძნებულია ცისტეამინით მორთულ ოქროს ნანონაწილაკებზე (Cyst/AuNPs), სმარტფონზე დაფუძნებულ ბიოსენსორთან ერთად, რაც საშუალებას იძლევა სიმსივნეების ფართო სპექტრის სწრაფი ადრეული სკრინინგის. ლეიკემიის ადრეული სკრინინგი შეიძლება ჩატარდეს სისხლის ნიმუშიდან დნმ-ის ექსტრაქციიდან 15 წუთის განმავლობაში, 90.0%-იანი სიზუსტით. სტატიის სათაურია „ადამიანის სისხლში კიბოს დნმ-ის სწრაფი აღმოჩენა ცისტეამინით დაფარული AuNPs-ისა და მანქანური სწავლების მხარდაჭერით აღჭურვილი სმარტფონის გამოყენებით“.
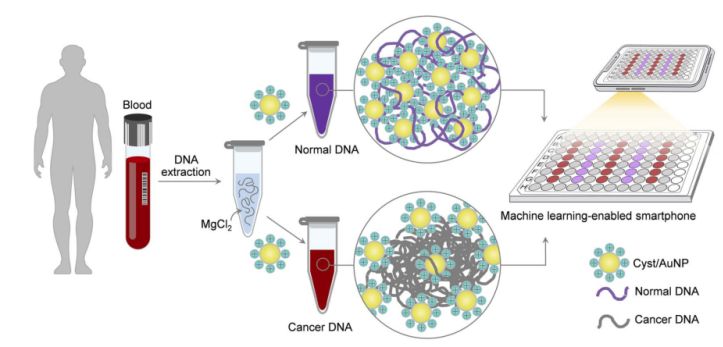
სურათი 1. კისტის/AuNPs კომპონენტების მეშვეობით კიბოს სკრინინგის მარტივი და სწრაფი ზონდირების პლატფორმის შექმნა შესაძლებელია ორ მარტივ ეტაპად.
ეს ნაჩვენებია ნახაზ 1-ში. თავდაპირველად, დნმ-ის ფრაგმენტების გასახსნელად გამოყენებული იქნა წყალხსნარი. შემდეგ შერეულ ხსნარს დაემატა კისტა/AuNP-ები. ნორმალურ და ავთვისებიან დნმ-ს განსხვავებული მეთილირების თვისებები აქვს, რაც იწვევს დნმ-ის ფრაგმენტებს სხვადასხვა თვითაწყობის ნიმუშებით. ნორმალური დნმ თავისუფლად აგრეგირდება და საბოლოოდ აგრეგირებს კისტას/AuNP-ებს, რაც იწვევს კისტას/AuNP-ების წითლად გადახრილ ბუნებას, ისე, რომ ფერის შეცვლა წითელიდან იისფერში შეიძლება შეინიშნოს შეუიარაღებელი თვალით. ამის საპირისპიროდ, კიბოს დნმ-ის უნიკალური მეთილირების პროფილი იწვევს დნმ-ის ფრაგმენტების უფრო დიდი კლასტერების წარმოქმნას.
96-ჭეჭიანი ფირფიტების სურათები გადაღებულია სმარტფონის კამერის გამოყენებით. კიბოს დნმ გაიზომა მანქანური სწავლების ფუნქციით აღჭურვილი სმარტფონით, სპექტროსკოპიაზე დაფუძნებულ მეთოდებთან შედარებით.
კიბოს სკრინინგი რეალურ სისხლის ნიმუშებში
სენსორული პლატფორმის სარგებლიანობის გასაფართოებლად, მკვლევარებმა გამოიყენეს სენსორი, რომელიც წარმატებით ასხვავებდა ნორმალურ და სიმსივნურ დნმ-ს რეალურ სისხლის ნიმუშებში. CpG უბნებზე მეთილირების ნიმუშები ეპიგენეტიკურად არეგულირებს გენების ექსპრესიას. კიბოს თითქმის ყველა ტიპში დნმ-ის მეთილირების და შესაბამისად, სიმსივნის გენების ექსპრესიის ცვლილებები მონაცვლეობით შეინიშნება.
დნმ-ის მეთილირებასთან დაკავშირებული სხვა კიბოს მოდელების მოდელად, მკვლევარებმა გამოიყენეს ლეიკემიით დაავადებული პაციენტებისა და ჯანმრთელი საკონტროლო ჯგუფის სისხლის ნიმუშები, რათა შეესწავლათ მეთილირების ლანდშაფტის ეფექტურობა ლეიკემიური კიბოს დიფერენცირებისას. მეთილირების ლანდშაფტის ეს ბიომარკერი არა მხოლოდ აღემატება ლეიკემიის სკრინინგის არსებულ სწრაფ მეთოდებს, არამედ აჩვენებს ამ მარტივი და პირდაპირი ანალიზის გამოყენებით კიბოს ფართო სპექტრის ადრეული გამოვლენის შესაძლებლობას.
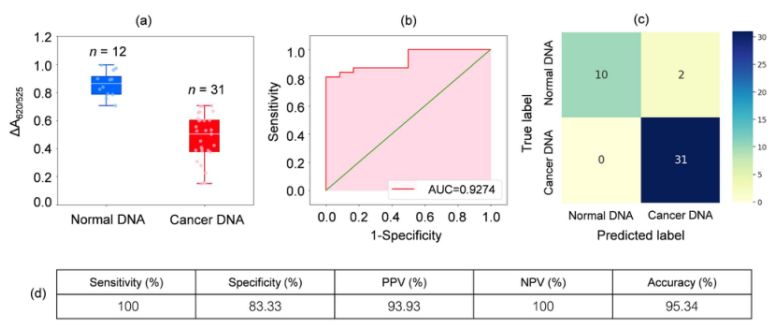
გაანალიზდა 31 ლეიკემიით დაავადებული პაციენტისა და 12 ჯანმრთელი პირის სისხლის ნიმუშებიდან აღებული დნმ. როგორც ნაჩვენებია ნახაზი 2ა-ზე მოცემულ ჩარჩო დიაგრამაზე, კიბოს ნიმუშების ფარდობითი შთანთქმა (ΔA650/525) უფრო დაბალი იყო, ვიდრე ნორმალური ნიმუშების დნმ-ისა. ეს ძირითადად განპირობებული იყო გაძლიერებული ჰიდროფობიურობით, რაც იწვევდა კიბოს დნმ-ის მკვრივ აგრეგაციას, რაც ხელს უშლიდა ცისტების/AuNP-ების აგრეგაციას. შედეგად, ეს ნანონაწილაკები მთლიანად გაიფანტა კიბოს აგრეგატების გარე ფენებში, რამაც გამოიწვია ნორმალური და კიბოს დნმ-ის აგრეგატებზე ადსორბირებული ცისტების/AuNP-ების განსხვავებული დისპერსია. შემდეგ ROC მრუდები გენერირდებოდა ზღურბლის მინიმალური მნიშვნელობიდან ΔA650/525 მაქსიმალურ მნიშვნელობამდე ცვალებადობით.
სურათი 2.(ა) კისტის/AuNPs ხსნარების ფარდობითი შთანთქმის მნიშვნელობები, რომლებიც აჩვენებს ნორმალური (ლურჯი) და კიბოს (წითელი) დნმ-ის არსებობას ოპტიმალურ პირობებში.
(DA650/525) კვადრატული დიაგრამების; (ბ) დიაგნოსტიკური ტესტების ROC ანალიზი და შეფასება. (გ) ნორმალური და კიბოთი დაავადებული პაციენტების დიაგნოზის დასმისთვის კონფუზიის მატრიცა. (დ) შემუშავებული მეთოდის მგრძნობელობა, სპეციფიკურობა, დადებითი პროგნოზირებადი მნიშვნელობა (PPV), უარყოფითი პროგნოზირებადი მნიშვნელობა (NPV) და სიზუსტე.
როგორც ნაჩვენებია ნახაზ 2b-ზე, შემუშავებული სენსორისთვის მიღებულმა ROC მრუდის ქვეშ არსებულმა ფართობმა (AUC = 0.9274) აჩვენა მაღალი მგრძნობელობა და სპეციფიკურობა. როგორც ჩარჩოს დიაგრამიდან ჩანს, ნორმალური დნმ-ის ჯგუფის წარმომადგენელი ყველაზე დაბალი წერტილი კარგად არ არის გამოყოფილი კიბოს დნმ-ის ჯგუფის წარმომადგენელი ყველაზე მაღალი წერტილისგან; ამიტომ, ნორმალური და კიბოს ჯგუფების დიფერენცირებისთვის გამოყენებული იქნა ლოგისტიკური რეგრესია. დამოუკიდებელი ცვლადების ნაკრების გათვალისწინებით, ის აფასებს მოვლენის, როგორიცაა კიბო ან ნორმალური ჯგუფი, ალბათობას. დამოკიდებული ცვლადი მერყეობს 0-დან 1-მდე. შესაბამისად, შედეგი არის ალბათობა. ჩვენ განვსაზღვრეთ კიბოს იდენტიფიკაციის ალბათობა (P) ΔA650/525-ის საფუძველზე შემდეგნაირად.
სადაც b=5.3533, w1=-6.965. ნიმუშის კლასიფიკაციისთვის, 0.5-ზე ნაკლები ალბათობა ნორმალურ ნიმუშზე მიუთითებს, ხოლო 0.5 ან მეტი ალბათობა კიბოს ნიმუშზე მიუთითებს. სურათი 2c ასახავს კლასიფიკაციის მეთოდის სტაბილურობის დასადასტურებლად გამოყენებული ჯვარედინი ვალიდაციის შედეგად გენერირებულ დაბნეულობის მატრიცას. სურათი 2d აჯამებს მეთოდის დიაგნოსტიკური ტესტის შეფასებას, მათ შორის მგრძნობელობას, სპეციფიკურობას, დადებით პროგნოზირებად მნიშვნელობას (PPV) და უარყოფით პროგნოზირებად მნიშვნელობას (NPV).
სმარტფონზე დაფუძნებული ბიოსენსორები
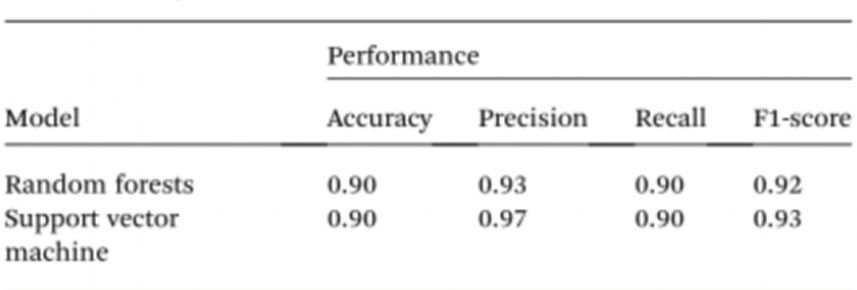
სპექტროფოტომეტრების გამოყენების გარეშე ნიმუშის ტესტირების კიდევ უფრო გასამარტივებლად, მკვლევარებმა გამოიყენეს ხელოვნური ინტელექტი (AI) ხსნარის ფერის ინტერპრეტაციისა და ნორმალური და სიმსივნური პირების გასარჩევად. ამის გათვალისწინებით, კომპიუტერული ხედვა გამოიყენეს Cyst/AuNPs ხსნარის ფერის ნორმალურ დნმ-ად (იისფერი) ან სიმსივნურ დნმ-ად (წითელი) გადასათარგმნად, მობილური ტელეფონის კამერით გადაღებული 96-ჭაბურღილიანი ფირფიტების სურათების გამოყენებით. ხელოვნურ ინტელექტს შეუძლია შეამციროს ხარჯები და გააუმჯობესოს ხელმისაწვდომობა ნანონაწილაკების ხსნარების ფერის ინტერპრეტაციაში, სმარტფონის ნებისმიერი ოპტიკური აპარატურის აქსესუარების გამოყენების გარეშე. და ბოლოს, მოდელების ასაგებად გაწვრთნილი იქნა ორი მანქანური სწავლების მოდელი, მათ შორის Random Forest (RF) და Support Vector Machine (SVM). როგორც RF, ასევე SVM მოდელებმა სწორად დაახარისხეს ნიმუშები, როგორც დადებითი და უარყოფითი, 90.0%-იანი სიზუსტით. ეს იმაზე მიუთითებს, რომ ხელოვნური ინტელექტის გამოყენება მობილურ ტელეფონზე დაფუძნებულ ბიოსენსორულ კვლევაში სავსებით შესაძლებელია.
სურათი 3. (ა) გამოსახულების მიღების ეტაპისთვის ნიმუშის მომზადების დროს დაფიქსირებული ხსნარის სამიზნე კლასი. (ბ) გამოსახულების მიღების ეტაპის დროს გადაღებული სამაგალითო სურათი. (გ) გამოსახულებიდან ამოღებული 96-ჭედიანი ფირფიტის თითოეულ ჭაში კისტის/AuNPs ხსნარის ფერის ინტენსივობა (ბ).
Cyst/AuNP-ების გამოყენებით, მკვლევარებმა წარმატებით შეიმუშავეს მეთილირების ლანდშაფტის აღმოჩენის მარტივი სენსორული პლატფორმა და სენსორი, რომელსაც შეუძლია ნორმალური დნმ-ის კიბოს დნმ-ისგან გარჩევა ლეიკემიის სკრინინგისთვის რეალური სისხლის ნიმუშების გამოყენებისას. შემუშავებულმა სენსორმა აჩვენა, რომ რეალური სისხლის ნიმუშებიდან ამოღებული დნმ-ს შეეძლო ლეიკემიით დაავადებულ პაციენტებში კიბოს დნმ-ის მცირე რაოდენობით (3 ნმ) სწრაფად და ეკონომიურად აღმოჩენა 15 წუთში და აჩვენა 95.3%-იანი სიზუსტე. ნიმუშის ტესტირების კიდევ უფრო გასამარტივებლად და სპექტროფოტომეტრის საჭიროების აღმოსაფხვრელად, გამოყენებული იქნა მანქანური სწავლება ხსნარის ფერის ინტერპრეტაციისა და ნორმალური და კიბოთი დაავადებული პირების მობილური ტელეფონის ფოტოს გამოყენებით დიფერენცირებისთვის. სიზუსტის მიღწევა ასევე შესაძლებელი გახდა 90.0%-ით.
მითითება: DOI: 10.1039/d2ra05725e
გამოქვეყნების დრო: 2023 წლის 18 თებერვალი
 中文网站
中文网站